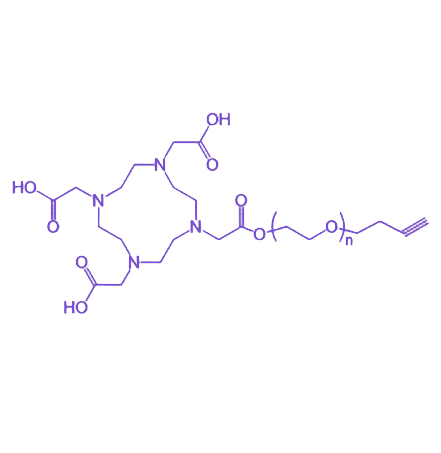
DOTA-PEG-Alkyne 是一种整合了 DOTA 大环配体、PEG 链段与 炔基 反应基团的多功能化合物,通过协同发挥各组分特性,在生物医学及材料科学领域展现出重要应用价值。其核心结构设计使其既能实现金属离子络合,又具备亲水性调节及高效生物偶联能力,为靶向成像、药物递送及功能材料构建提供关键连接工具。
作为十二元四氮杂大环配体,DOTA 单元对 Gd³⁺、Lu³⁺、In³⁺、Cu²⁺、Y³⁺ 等多种金属离子具有优异的配位能力,可形成热力学稳定的金属络合物,这一特性使其在 医学成像(如MRI对比剂、核素显像)和 靶向药物递送 中成为核心功能模块。通过络合不同金属离子,可赋予化合物诊断或治疗双重功能,满足精准医疗需求。
分子链中的 PEG(聚乙二醇)链段作为生物相容性调节剂,显著提升化合物的 水溶性 和 循环稳定性。其亲水性本质有效减少生物体内的非特异性蛋白吸附,降低免疫原性,延长血液半衰期,为体内应用提供优化的药代动力学特性。PEG链长可根据需求调整,进一步调控化合物的理化性质及生物分布行为。
末端修饰的 炔基 基团赋予分子高效的 点击化学反应活性,可通过 铜催化叠氮-炔环加成(CuAAC) 或 无铜点击反应(如与 DBCO 等环张力炔烃的 SPAAC 反应),与含叠氮基(-N₃)的生物分子(如抗体、肽、核酸)或纳米载体快速偶联,形成稳定的三唑环连接。这种反应具有高选择性、高产率及温和反应条件的特点,适用于复杂生物体系中的精准修饰。
凭借独特的结构优势,DOTA-PEG-Alkyne 在 生物分子功能化、纳米材料表面修饰 及 多功能药物递送系统构建 中发挥桥梁作用。例如,通过炔基与叠氮修饰的抗体偶联,同时利用 DOTA 络合放射性核素,可制备兼具靶向识别与核素治疗功能的生物偶联药物;或通过修饰纳米颗粒表面,实现成像引导下的精准药物释放,为疾病诊断与治疗的一体化提供创新解决方案。


 渝公网安备
渝公网安备 